Trattamento endovascolare stenosi della carotide
Introduzione
Il punto fondamentale di questo tipo d’intervento è la valutazione del paziente, per capire se la sua lesione carotidea è a rischio embolico durante l’intervento; l’esperienza dell’operatore e l’utilizzo di un ampio ventaglio di soluzioni tecniche, sia in fase diagnostica, che durante l’intervento, consente di scegliere il presidio più appropriato, per effettuare l’intervento in sicurezza.
[L’arteria carotide è situata nel collo; ogni essere umano ha due carotidi, una per lato, la destra e la sinistra; nascono alla base del collo, dall’arco aortico, posto all’interno del torace; a livello dell’angolo mandibolare, si dividono in due rami: la carotide esterna, per la cute e i tessuti della faccia, e la carotide interna, per il cervello. Il cervello riceve il sangue sia anteriormente, dalle carotidi interne, sia posteriormente, dalle arterie vertebrali.
Un’alterazione della carotide può comportare lesioni importanti a valle, come TIA e stroke; il suo trattamento ha l’obiettivo di ridurre i rischi di tali alterazioni, debilitanti, non certo di curare gli eventi avvenuti. Lo stoke può essere emorragico o ischemico; in questo secondo caso, la riduzione di flusso ematico ne è alla base; il restringimento del lume dell’arteria carotide interna, la costituzione di una placca ulcerata, l’indurimento della parete arteriosa per depositi calcifici sono tutte espressioni della malattia arteriosclerotica, che favoriscono la creazione di coaguli, più o meno grandi, che possono essere trasportati, improvvisamente o molto lentamente, verso il cervello, causando lo stoke o il TIA. La presenza di una sintomatologia neurologica e la concomitante esistenza di una lesione carotidea, nel lato dei sintomi, obbliga a trattare la lesione; le la stenosi è sotto il 50% ed è isolata, potrebbe essere sufficiente la terapia medica; se la stenosi è associata ad una lesione controlaterale, allora va trattata; per gradi più severi di stenosi, il trattamento non solo medico è obbligatorio.]
Epidemiologia
Il 20-40% degli ictus cerebrali è legato alla presenza di lesioni ateromasiche, a livello della biforcazione carotidea, in sede extracranica. Alcuni studi randomizzati hanno dimostrato che la rimozione chirurgica della placca, mediante endoarteriectomia, è superiore alla terapia medica antiaggregante nella prevenzione dell’ictus, in caso di lesioni che determinano una stenosi superiore al 60%, in pazienti con una sintomatologia correlata alla lesione, oppure superiore al 70-80% in pazienti asintomatici. [North American Symptomatic Carotid Endoarterectomy Trial Collaboration. Beneficial effect of carotid endoarterectomy in symptomatic patients with high grade carotid stenosis. N Engl J Med 1991; 325: 445-453.]
Dopo le pioneristiche esperienze di Mathias, con la sola PTA, oggi il trattamento implica l’impianto di uno stent. Inizialmente, il trattamento con stent era riservato solo ai pazienti con stenosi significative, che presentavano un aumentato rischio operatorio, per occlusione della carotide controlaterale, per lesioni molto distali non facilmente raggiungibili con la chirurgia, per la presenza di comorbilità cardiache e respiratorie. Da queste indicazioni restrittive si è passati ad un’applicazione elettiva per quasi tutti i pazienti, con poche controindicazioni, quali la presenza di un trombo fresco o di lesioni intracraniche. L’ampliamento delle indicazioni è dovuto ad una progressiva diminuzione delle complicazioni neurologiche, per la migliore applicazione della tecnica di stenting e per il sistematico impiego dei mezzi di protezione cerebrale. [Mathias K. Perkutane transluminale Katheterbehandlung supraaortaler arterienobstruktionen. Angio 1981; 3: 47-50. + Roubin SG, New G, Iyer SS. Et al. Immediate and late clinical outcomes of carotd artery stenting in patients with symptomatic and asymptomatic carotid artery stenting. A 5-year prospective analysis. Circulation 2001; 103: 532-537. + Cremonesi A, Castriota F. Efficacy of a nitinol filter devicein the prevention of embolic events during carotid interventions. J Endovascular Ther 2002; 9: 155-159.].
Indicazioni
[Il primo trattamento da effettuare è quello medico: oltre al controllo dei fattori di rischio e all’effettuazione di un costante esercizio fisico, la terapia medica si basa sugli antiaggreganti (dal momento che il sangue contiene piastrine, responsabili dell’aggregazione cellulare e della formazione dei trombi, molto utile in caso di sanguinamento, queste possono essere spinte a non aggregarsi, rendendo difficoltoso l’aggregazione cellulare – Tiklid, Persantin, Clopidogrel) – sull’impiego di statine (la loro azione si rivolge ad evitare l’accumulo di colesterolo; vengono accoppiate all’alimentazione ricca di verdure e di frutta; la lunga assunzione può comportare facile affaticamento muscolare, modificazione degli indici di funzionalità epatica + il secondo trattamento proposto è quello chirurgico (l’endoarteriectomia ha lo scopo di rimuovere la malattia); una soluzione facile per il chirurgo, vista la superficailità dell’arteria. + lo stent carotideo (è l’ultima opzione presentata, ma che sta conquistando sempre più spazio)]
Paziente sintomatico, con una lesione unilaterale maggiore del 50% e sintomatologia neurologica correlata per lato, registrata negli ultimi 6 mesi. Paziente asintomatico con una lesione maggiore del 80%. Presenza di fattori di rischio che orientano verso la soluzione endovascolare: clinici [età superiore a 75 anni, classe NYHA III e IV, coronaropatia con molteplici localizzazioni, insufficienza respiratoria, lesione nervosa controlaterale], anatomici [lesione cervicale alta rispetto alla mandibola, lesione tandem, restenosi dopo endoarteriectomia, occlusione carotide interna controlaterale, collo ostile per precedente radioterapia, o intervento chirurgico per altre motivazioni o collo taurino, o immobilizzazione del collo].
Anatomia vascolare
Lo studio dell’anatomia vascolare comprende tre settori anatomici: l’analisi dei vasi carotidei [occorre conoscere il diametro trasverso dei vasi carotidei, nel punto in cui il vaso si biforca e da origine alle due carotidi, la lunghezza della malattia, le caratteristiche della stenosi: l’entità, la presenza della componente calcifica, il tipo di placca – la placca vulnerabile, o ad elevato rischio embolico, si presenta allungata, a superficie irregolare o profondamente ulcerata, in grado di essere ricettacolo di materiale embolico responsabile dei fenomeni ischemici transitori che richiamano l’attenzione del clinico – oppure può essere a superficie regolare, composta da un aggregato lipidico, ricoperta da una sottile capsula fibrosa, estremamente pericolosa in corso d’intervento – oppure può essere fibrosa e non destare sospetti. Una classificazione della loro vulnerabilità può essere effettuata con l’eco-color-Doppler in grado di differenziare la minore ecogenicità della placca vulnerabile + Verhoven BA, deVnes JP, Pasterkamp G, et al. Carotid atherosclerotic plaque characteristic are associated with microembolization during carotid endoarterectomy and procedural outcome. Stroke 2005; 36: 1735-40. + Biasi GM, Froio A, Dietrich EB, et al. Carotid plaque echolucency increas the risk of stroke in carotid stenting: the imaging in carotid angioplasty and risks of stroke (ICAROS) study. Circulation 2004; 110: 756-62. – Occorre inoltre sapere l’angolazione e la tortuosità dei vasi: il ripiegamento, kinking, o l’andamento spiraliforme, coiling; questi possono rendere complicato l’avanzamento dello stent, per cui occorre rettilineizzarle prima], la classificazione dell’arco aortico [l’arco aortico è classificato sulla base della distanza dell’origine del tronco brachiocefalico dal vertice dell’arco aortico: il punto in cui la arteria carotide comune sinistra è più ampia viene preso come punto di riferimento. Occorre la proiezione obliqua anteriore sinistra per visualizzare e classificare l’arco aortico. La distanza verticale tra il tronco brachiocefalico e la sommità dell’arco aortico determina il tipo di arco; nel tipo 1, tale distanza è inferiore a 1 diametro dell’arteria carotide comune sinistra, nel tipo 2 tale distanza è tra 1 e 2 diametri dell’arteria carotide comune sinistra, mentre nel tipo 3, tale distanza è superiore a 2 diametri dell’arteria carotide comune sinistra. Questa classificazione riflette la difficoltà tecnica per il cateterismo selettivo del vaso e, quindi, per il posizionamento di un supporto per il passaggio dei presidi da impiegare, in grado di essere stabile, evitare la caduta all’interno dell’aorta ascendente – inoltre va evidenziata la presenza di irregolarità sull’arco aortico stesso, anche calcifiche, specie in prossimità della loro origine, dove maggiore è il contatto con i cateteri e il rischio di origine del materiale embolico, ma anche di una eventuale dissezione], la visualizzazione del compenso intracranico [l’integrità del circolo di Willis è fondamentale per conoscere la possibilità dei circoli collaterali; i rami comunicanti anteriori e posteriori consentono la possibilità del flusso controlaterale; la presenza di una lesione nell’arteria cerebrale media obbliga a trattare la lesione a valle, prima d’intraprendere il trattamento della biforcazione carotidea; inoltre consente di escludere la presenza di varianti anatomiche].
I fattori che rendono difficoltosa l’effettuazione di un intervento endovascolare sono: la tortuosità e la calcificazione delle arterie iliache [possono rendere difficile ecomplicato il passaggio e la stabilità di un introduttore lungo 8-9Fr], la presenza di lesioni all’ostio della carotide comune [che va trattata prima, non nella stessa seduta], la presenza di placche calcifiche [rendono possibile una dissezione durante il passaggio del materiale].
Diagnosi
La semplice diagnosi di presenza o meno di una stenosi carotidea, con la sua gradazione, può essere affidata all’eco-color-Doppler, in grado di rappresentare morfologicamente e funzionalmente la stenosi, arrivando a determinare l’entità.
A supporto dell’intervento endovascolare occorrono altre informazioni che solo l’angio TC, o l’angio RM, possono fornire, oltre alla valutazione neurologica.
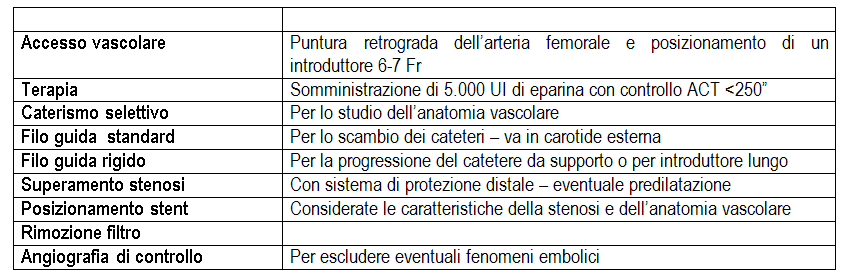 Bohannon W T. Technical tips for catotid angioplasty and stenting. Sem Vasc Surg 2008; 21: 3-7
Bohannon W T. Technical tips for catotid angioplasty and stenting. Sem Vasc Surg 2008; 21: 3-7
Intervento
Inizialmente, Mathias, a Dortmund, applicava al trattamento della stenosi carotide la sua esperienza nell’interventistica periferica, per cui passava la stenosi con un filo guida 0,035”, posizionava il catetere a palloncino e lo stent, sulla base dei reperi ossei della colonna vertebrale, anche senza visualizzare la stenosi.
protocollo farmacologico
Il paziente è stato preparato con aspirina (125 mg) e ticlopidina (250 mg per 2 al dì), almeno tre giorni prima della procedura + non deve sospendere la terapia anti-ipertensiva; il giorno dell’intervento, oltre a monitorare i parametri vitali, oltre ad idratare il paziente, si valuta la risposta neurologica con un giocarello posto nella mano controlaterale alla sede dell’intervento, che il paziente ciclicamente aziona + al momento dell’inserimento dell’introduttore vascolare femorale e prima delle manovre d’incannulamento della carotide, s’infonde eparina (70-100 U/kg), che ha un tempo di dimezzamento di 30-45’. Al termine della procedura, se l’ACT supera i 250”, si può antagonizzare l’eparina con la somministrazione di solfato di protamina, per il rischio di emorragie intracraniche. Nel follow-up continua ad assumere aspirina a tempo indeterminato, con ticlopidina, o altri antiaggreganti, per 1 mese.
accesso vascolare
1°: arteria femorale destra, che permette un’agevole incannulazione delle arterie carotidi comuni.
2°: arteria brachiale, in caso di occlusione delle arterie femorali comuni o iliache – la brachiale destra, per un intervento nella carotide comune sinistra e viceversa.
3°: arteria radiale: viste le dimensioni dei cateteri guida da impiegare e la possibilità di uno spasmo protratto, con possibile trombosi, è preferibile non impiegare tale accesso.
Valutazione angiografica di base
Angiografia dell’arco aortico, con visualizzazione dell’emergenza e dell’iniziale decorso dei vasi epiaortici: la proiezione è obliqua anteriore sinistra di 30-40°.
Angiografia selettiva delle due carotidi, con visualizzazione extracranica dell’arteria carotide comune [biforcazione carotidea + carotide interna ed esterna – proiezione laterale per la sinistra e OAD per la destra; serve a dimostrare le caratteristiche della stenosi e il decorso dei vasi, oltre a consentire la valutazione dei diametri] ed intracranica [proiezione A-P e laterale – serve ad escludere una eventuale malformazione cerebrale, come confronto per escludere fenomeni embolici, verifica se un’occlusione prossimale è fattibile]. Il completamento dello studio prevede anche il cateterismo selettivo delle arterie vertebrali, per confermare l’adeguatezza del compenso fornito dal circolo collaterale e dal poligono di Willis.
Chiaramente, dopo un preventivo studio angio TC, con le ricostruzioni multiplanari, solo lo studio intracranico rimane fa effettuare al momento dell’intervento.
cateteri diagnostici
Il cateterismo selettivo dell’arteria carotide comune, con un catetere angiografico diagnostico è necessario per acquisire le immagini di dettaglio della biforcazione carotidea e del tipo di stenosi e per favorire l’ingresso di guide di supporto.
Judkins curva destra, l’Amplatz destro [per origini acute dell’arteria carotide comune sinistra], mammaria interna [per l’accesso brachiale o radiale], l’Headhunter, il Simmons I o II [consentono d’incannulare stabilmente le carotidi più difficili. Grazie alla curva del catetere, posizionata a livello dell’aorta ascendente o nell’arco aortico].
Salvo che per casi molto semplici, è preferibile avanzare il catetere diagnostico, solo dopo aver portato il filo guida 0,035” [idrofilica, Terumo, punta J, flessibile per 3 cm in punta, poco traumatica nella versione standard] in carotide esterna.
Lo studio angiografico carotideo è parte integrante dell’intervento [in questa fase possono essere prodotte delle piccole lesioni, asintomatiche, dovute alla dislocazione di frammenti di placca, dall’arco aortico o dagli osti delle arterie carotidi – è consigliabile effettuare una panoramica toracica e dell’arco, in proiezione obliqua sinistra; a completamento non deve mancare lo studio panoramico, in antero-posteriore e in laterale, del circolo intracranico, per avere informazioni sull’esistenza di lesioni stenotiche intracraniche, sul grado di vascolarizzazione endocranica, utili per il confronto al termine dell’intervento. La pressione di perfusione può essere portata cautelativamente a 600 PSI.].
Lo studio carotideo selettivo può essere effettuato con un Headhunter o un Simmons I o II, per il tronco anonimo e per la carotide sinistra, se l’arco è stretto e il percorso dei vasi è rettilineo [ l’ingresso del catetere nel vaso, preceduto dal filo guida, il cui percorso va seguito direttamente, fino al suo parcheggio in arteria carotide esterna, deve essere controllato, con uno sguardo al suo passaggio tra arco e carotide; la lesione stenotica non andrebbe attraversata in questa fase; la punta del catetere diagnostico non deve oltrepassare il terzo distale della carotide comune, per effettuare lo studio panoramico extra ed intracranico; un volta scelta la proiezione migliore, dove la biforcazione carotidea è quasi a canna di fucile. A questo punto, il catetere è spinto in carotide esterna, si effettua lo scambio di fili guida: da una standard ad una rigida; a questo punto, si porta il catetere da lavoro: introduttore lungo o catetere guida].
accesso in arteria carotide
Elemento cardine dell’intervento è poter conseguire l’accesso all’arteria carotide comune, nel lato da trattare, con un introduttore lungo [La prima causa dell’insuccesso della procedura endovascolare è proprio l’impossibilità ad avanzare uno dei due presidi per una caratteristica dell’arco aortico, o per il coiling o il kinking della carotide.], o con un catetere guida. L’intento è quello di conseguire una posizione stabile e sicura, per poter poi effettuare agevolmente i vari passaggi di materiale, senza dover ricorrere ad alcuno sforzo, e concludere l’intervento percutaneo.
L’introduttore lungo è lo strumento preferito dalla scuola francese [6 o 7 Fr, 80-90 cm, prevede il preventivo ingresso del catetere diagnostico su filo guida 0,035”, magari con la tecnica “push and pull”, per superare eventuali difficoltà; successivamente si cambia guida, con una lunga 260 cm, stesso calibro, più rigida, la cui punta è parcheggiata in carotide esterna – la tecnica radiologica del “road mapping” consente di vedere i vasi, senza ulteriore iniezione di mezzo di contrasto. Una volta che il filo guida è in posizione di sicurezza, si sfila il catetere diagnostico e si inserisce l’introduttore lungo; particolare attenzione è diretta al momento del passaggio dall’arco aortico in carotide, da osservare direttamente in scopia. In casi di curve molto angolate, può essere utile rimuovere parzialmente il dilatatore interno, in modo da offrire meno resistenza alla progressione del complesso. L’introduttore è avanzato fino a poco prima della biforcazione carotidea. Dilatatore interno e filo guida vengono rimossi; l’introduttore è collegato ad un sistema di lavaggio eparinato, a pressione. Ci sono gli introduttori armati dell’Arrow, o quelli più flessibili della Cook, gli shuttle.]. Questa tecnica prevede più passaggi [catetere diagnostico, incannulazione carotide esterna con guida di supporto e da scambio, introduttore definitivo – per effettuare un cateterismo selettivo di una carotide da un arco di tipo III, è preferibile un Judkins 2 o un Simmons II o III]; ha il vantaggio di una progressione controllata dall’aorta, con la punta rastremata del dilatatore, in modo da non creare scalini pericolosi, in grado di mobilitare porzioni di placca e possibili embolizzazioni cerebrali; non secondario è il maggior supporto per completare lo stenting.
Il catetere guida, 7-8 Fr è il secondo, ma anche più economico, modo di accedere alle arterie carotidi [si può impiegare il catetere guida con una curvatura tipo per la mammaria se si vuole entrare nella carotide comune sinistra, o il multipurpose per entrare a destra; in genere si avanzano tali presidi, facendoli scorrere sulla guida 0,035”, grazia anche ai primi 5 cm molto morbidi, tipo Guider della Boston – giunti all’arco aortico, si effettua la rotazione del catetere, con il filo guida inserito, in modo da farla progredire in carotide comune e costruire il binario su cui fare scorrere il catetere guida, con un meccanismo “pull and push”; per prendere la carotide sinistra, il catetere viene ritirato delicatamente e ruotato leggermente in avanti, vista la sua posizione più anteriore; viceversa è ruotato posteriormente in un arco allungato. Possono essere necessarie due guide per fare progredire il catetere guida su un supporto più stabile. Una volta raggiunta la posizione ideale, per garantire stabilità, un filo guida 0,014” può essere lasciato stabilmente in arteria carotide esterna, lasciano all’altro filo guida 0,014” il compito di portare a termine l’intervento – è buona norma aspirare il contenuto, dopo la rimozione della guida, per evitare l’introduzione di eventuali microbolle aeree + effettuare un lavaggio continuo con soluzione fisiologica eparinizzata]. Ha il vantaggio di essere molto più semplice, veloce ed economico; comporta un rischio di embolizzazione in caso di arco aortico con severe apposizioni ateromasiche. In tutti i casi consigliamo di sospendere tutti i tentativi se dopo 30’ do attività non si è riusciti ad incannulare selettivamente la carotide: occorre rivalutare il trattamento chirurgico.
sistemi di protezione
In tutte le procedure endovascolari esiste la possibilità di una embolizzazione distale del materiale trombotico esistente; chiaramente, questo fatto acquista una maggiore importanza ed evidenza nel territorio cerebrale. Le placche instabili, con la ricchezza di materiale trombotico friabile, possono essere mobilizzate durante il passaggio dei presidi dedicati, con il rilascio di micro (meno di 100 micron) o macroemboli (maggiori di 200 micron); questi ultimi sono associati con eventi clinici importanti, mentre i primi possono essere associati con cambiamenti nelle funzioni cognitive.
I risultati dei vari studi clinici, oltre a confermarci che lo stenting carotideo è associato ad una maggiore embolizzazione di frammenti rispetto all’endoarteriectomia chirurgica, [Jordan WD, Voellinger DC, Doblar DD, et al. Microemboli detected by transcranial Doppler monitoring in patients duuring carotid angioplsty versus carotidendoarterectomy. Cardiovasc Surg 1999; 7: 33-38.] ci confermano che l’adozione dei sistemi di protezione cerebrale comporta una diminuzione del 70% delle complicazioni emboliche; la scelta tra sistema di protezione distale o prossimale dipende dallo stato della sintomatologia del paziente, dall’anatomia dei vasi da attraversare e dalle caratteristiche della placca carotidea.
I sistemi di protezione distali possono essere, a loro volta, classificati in eccentrici [il filtro si apre in posizione eccentrica rispetto al filo guida –sembrano essere indipendenti dal filo guida – hanno il vantaggio di aggiustare meglio il loro orientamento nei segmento tortuosi, a differenza dei concentrici, in modo da raggiungere il migliore adattamento al vaso – lo scheletro metallico è ricoperto di polietilene con fori, che consentono il passaggio del sangue, ma non degli emboli grossolani – possono determinare spasmo dell’arteria, oppure occlusione acuta, se tutti i pori vengono ricoperti dal materiale embolico; una buona antiaggregazione previene tale evenienza. Il basso profilo, la maneggevolezza, la flessibilità e l’adeguata apertura del filtro, per aderire bene alle pareti del vaso, sono le caratteristiche da osservare nella scelta del presidio – FilterWire BOSTON, Spider EV3] e concentrici [il filo guida è centrale rispetto al filtro – sono filtri montati su guida – una variante è il palloncino distale, montato su filo guida 0,014, Percusurge della medtronic, che viene gonfiato una volta giunto nella sede desiderata, per fare effettuare la procedura di PTA e stent; alla fine si avanza un catetere sulla stessa guida, per aspirare la colonna di sangue intrappolata sotto il palloncino, eliminando eventuali detriti. Alla fine si sgonfia il palloncino e si recupera la guida. Pur in presenza di un basso profilo, solo 2,2 Fr, e di una buona maneggevolezza, circa il 7% dei pazienti non sopporta tale occlusione del circolo e non è possibile visualizzare l’operato con l’iniezione di mezzo di contrasto, visto il blocco di flusso operato dal palloncino – Accunet ABBOTT, Angioguard CORDIS, Emboshield ABBOTT, Fibernet INVATEC (questo ha i pori più piccoli sul mercato e il profilo più piccolo) ], a seconda del loro comportamento rispetto al filo guida. Tutti vengono rilasciati, o aperti, o sguainati, nel tratto più rettilineo della carotide interna, per favorirne la massima apertura, il migliore adattamento al vaso. Tutti prevedono il superamento della stenosi in posizione compressa, all’interno del catetere portatore, per essere aperti, una volta giunti a destinazione [tale manovra può risultare difficile in caso di stenosi serrata o di andamento tortuoso o angolato del vaso; possono risultare utili i palloncini da dilatazione coronarica, da 2,5 mm, per aprire un importante varco, per continuare a lavorare in sicurezza] . Vengono recuperati, al termine della procedura di PTA/stent. Nelle placche ulcerate, o nei segmenti vascolari molto tortuosi, maggiore spazio hanno i filtri Spider EV3 ed Emboshield dell’Abbott [bare-wire filter]. La capacità di cattura degli emboli è in relazione alla porosità del materiale con cui è composto il filtro.
I sistemi di protezione prossimale basano la loro azione bloccando il flusso arterioso durante l’intervento; limitano o annullano l’afflusso di sangue dall’arteria carotide comune, invertendo il flusso dalla carotide esterna omolaterale [consentono di superare il limite di tutti i filtri distali: dover necessariamente oltrepassare la lesione stenotica, prima di poter essere aperti ed esplicare la loro funzione protettiva – un rischio che, seppure molto remoto, è presente. Per sopperire a questa “fase non protetta”, questi sistemi attuano una protezione doppia: un palloncino sarà posizionato in carotide comune e un palloncino, distante dal primo almeno 7 cm, in carotide esterna per bloccare del tutto il flusso anterogrado in carotide interna, sfruttando le connessioni vascolari cerebrali del poligono di Willis. Grazie all’occlusione operata dai palloncini, come se fosse un clampaggio endovascolare, il sistema è stabile e consente di lavorare in sicurezza; nella carotide comune ed esterna s’instaura una back pressure; dopo la procedura, prima di sgonfiare i palloncini, si recupera il sangue e i detriti. Il vantaggio è che tutta la procedura viene effettuata in sicurezza, non comporta dislocazioni di placche; lo svantaggio è rappresentato da un curva di apprendimento e dall’elevato calibro del presidio, 9 Fr – Moma invatec + Lo studio ARMOUR, studio della sicurezza del presidio in pazienti ad elevato rischio chirurgico, è multicentrico e prospettico; ha riportato eventi cerebrali nel 7,2% dei pazienti e un successo tecnico del presidio del 98% + Lo studio DESERVE, valutazione con RM dell’efficacia del filtro MoMa, è prospettico – Altro sistema è il Neuroprotection system, GORE, che mutua dal precedente il blocco della carotide comune e dell’esterna, l’inversione di flusso dalla carotide interna: questo flusso viene raccolto esternamente, filtrato, immesso di nuovo nel circolo venoso, attraverso un accesso femorale venoso, controlaterale alla sede di lavoro. + Lo studio EMPIRE, europeo, ha dimostrato la sicurezza del presidio, con 1.6% di eventi neurologici, su 122 pazienti trattati. – Il limite di entrambi è la necessità di dover ricorrere ad introduttori di calibro maggiore, rispetto ai distali; in pazienti con severa arteriopatia periferica, può comportare un incremento delle complicazioni della sede di accesso femorale (3% studio ARMOUR); si può registrare una intolleranza al clampaggio, per la presenza di uno scarso circolo collaterale intracranico e per un eccessivo tempo di chiusura, risolvibile questo con la curva di apprendimento. Si può risolvere ristabilendo la perfusione appena possibile, associare un filtro distale ed effettuare la procedura per gradi, provvedendo a sgonfiare e gonfiare i palloncini, per ogni gradino della procedura. Non ultimo, la presenza di alterazioni nella carotide controlaterale, che possono limitare il compenso del circolo di Willis.].
Come consigli di carattere generale, si può optare per un sistema di protezione prossimale in caso di assenza di uno spazio di atterraggio distale della carotide interna, in caso di complessa anatomia carotidea, in caso di stenosi ad elevato rischio embolico (placca ulcerata, stenosi sub-occlusiva lunga). Viceversa, nelle normali anatomie carotidee (biforcazione rettilinea), nelle lesioni stabili (posi-chirurgica o placca fibrosa) sono da preferire i sistemi distali.
L’introduzione di un sistema di protezione cerebrale deve avvenire molto delicatamente (per evitare spasmi dell’arteria), sotto diretto controllo radioscopico (per confermare la sede di posizione). La posizione ideale è a 3-4 cm dalla biforcazione carotidea e dalla stenosi da trattare; la conferma è con l’arteriografia nelle due proiezioni, per convalidare la piena apertura dello stesso [il presupposto dell’intervento è la concentrazione a livello della stenosi da trattare e della posizione del filtro, da mantenere stabile. Per questo è altrettanto importante, prima d’intraprendere questa fase che, nella precedente, ci si sia assicurati della stabilità del catetere guida o dell’introduttore lungo, in modo da non avere sorprese successivamente, che non prolassi all’interno dell’arco aortico, trascinandosi dietro il filtro e causando una dissezione o una embolizzazione dagli esisti disastrosi. Una proiezione obliqua dovrebbe garantire la visione comtemporanea di sistema filtro, stenosi e biforcazione aortica]. La stessa identica attenzione va ricolta al momento della rimozione dello stesso (in modo da non fare impigliare il filtro tra le maglie dello stent.
impianto stent
La predilatazione della stenosi carotidea è un momento delicato della procedura; visti i rischi connessi, deve essere effettuato dopo aver considerato il tipo di protezione cerebrale da applicare. Serve a superare una stenosi concentrica, molto elevata, che costuiterebbe un serio ostacolo alla progressione dello stent, specie se si ha un decorso tortuoso del vaso, per cui non si vuole avere problemi al successivo passaggio dello stent [preceduta da una infusione di 0,5-1 mg di atropina, 1’ prima del pallonamento, si attua con un catetere a palloncino, monorail o a ““rapid exchange”, 2.5-3 mm per 2 cm].
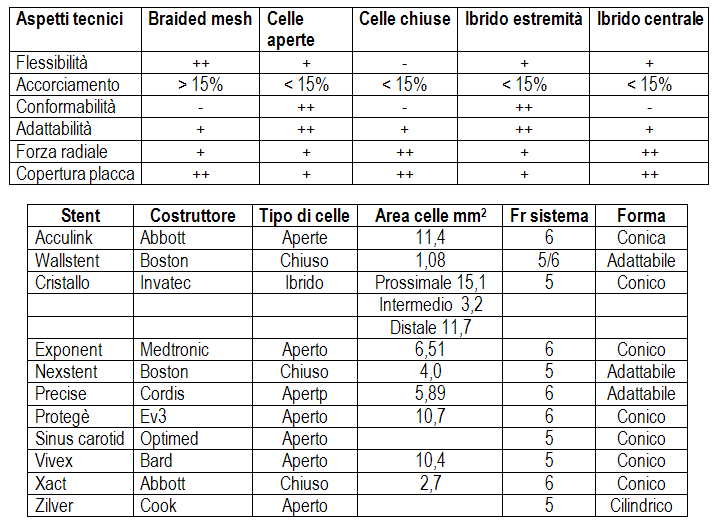
Tutti gli interventi prevedono l’impianto di uno stent [da una iniziale strategia di predilatazione, siamo passati allo stenting diretto. Solo in caso di lesioni molto severe, >90%, o calcifiche, o con una severa angolatura, che possono fare prevedere una difficoltà di progressione, allora si effettua una predilatazione con cateteri a palloncino di derivazione coronarica, di 2.5-3,5 Fr. Si utilizzano stent 6-8mm nelle donne e 7-9 mm negli uomini, prendendo come riferimento il diametro dell’arteria carotide comune distale, visto che il presidio ricoprirà la biforcazione, per atterrare in questo vaso, senza per questo comportare alterazioni di flusso in carotide esterna; solo nei casi in cui lo stent sarà rilasciato solo in arteria carotide interna, allora il calibro dello stent viene scelto sulla base del diametro di questo vaso. Vengono scelti stent lunghi, tanto da coprire agevolmente la lesione, garantendo ampie zone di atterraggio prossimale e distale, in genere 3-4 cm. Nella carotide s’impiegano solo stent autoespandibili. La tecnica prevede la prima apertura di 5 mm di stent, in modo da farlo aprire bene e aderire adeguatamente alle pareti della carotide e non farlo scivolare. L’assenza d’ingrandimento di visione durante la progressione dello stent lungo il tragitto nel tratto distale dell’aorta, consentirà di verificare l’assenza di ostacoli lungo il percorso. Una volta giunto al livello della carotide, si può tornare ad aumentare il campo di visione.]. Non occorre allungare lo stent per trattare anche una tortuosità del vaso; viceversa occorre evitare che la zona di atterraggio dello stent avvenga in una tortuosità; questa potrebbe piegare e chiudere lo stent.
Occorre considerare che nell’intervento chirurgico, il trombo viene rimosso; nell’intervento endovascolare questo viene compresso; per questo la geometria dello stent ha un intrinseco ruolo anti-embolizzazione: è capace d’influenzare il rischio di prolasso della placca e di embolizzazione periferica, durante tutto il periodo di epitelizzazione dello stent. Le caratteristiche delle superfici libere tra i vari elementi dello stent determinano l’impalcatura dello stent (scaffolding) e le capacità di copertura della parete del vaso [celle piccole consentono una maggiore copertura della placca, riducendone il rischio di una sua protrusione tra le maglie e di una successiva embolizazzione]..
Si dividono in acciaio o mesh-wire [il Carotid Wallstent è il più utilizzato; ha un profilo contenuto di 5,5 Fr, ha un corpo molto flessibile e la possibilità di uno scambio rapido della guida – grazie alla compressibilità, è contenibile in un introduttore, potendo essere sguainato al momento desiderato; ha il vantaggio di essere parzialmente recuperabile, per cui può essere riposizionato, se non si ritiene corretta la sua posizione – è a piccole celle, o strette, per cui garantisce una buona impalcatura, una buona capacità di adattamento alle caratteristiche del vaso; ha il limite di accorciarsi durante il rilascio e di essere rigido, dopo il rilascio.] o in nitinol [Precise della Cordis, Acculink della Guidant, X-act della Mednova, il Sinus della Biotronik – grazie alle proprietà termiche del metallo, si espandono alla forma costruita, una volta a contatto con la temperatura corporea; sono caratterizzati da una maggiore forza radiale e da una maggiore adattabilità al vaso, specie nel passaggio di calibro tra carotide comune ed interna. Non si accorciano, grazie alla costruzione anulare dello stent; sono a celle aperte, per cui si adattano meglio al decorso del vaso. Alcuni consentono il riposizionamento, alcuni hanno anche la conformazione conica, per venire incontro alle differenze di calibro tra carotide comune ed interna. Il limite è rappresentato dalla scarsa impalcatura e da una maggiore apertura, non in grado di contenere la placca. Non esistendo studi comparativi tra stent, non è possibile affermare se uno è superiore ad un altro.]. Uno stent ibrido è quello della Invatec, il Cristallo [presenta una struttura a celle aperte nelle estremità, dove è la zona di atterraggio dello stent; a livello centrale, dove aderisce alla placca, ci sono le celle chiuse: in questo modo si ottiene il giusto bilanciamento nell’impalcatura, nella capacità di coprire la placca – nel registro multicentrico prospettico la percentuale di stroke è stata 0. + Cremonesi A, Rubino P, Grattoni C, et al. Multicentre experience with a new kybrid carotid stent. J Endovasc Ther 2008; 15: 186-192.]. Lo stent può essere cilindrico o conico.
Non esiste uno stent applicabile per tutte le situazioni; la differenza nel disegno sta a dimostrare che in uno scenario non complicato [anatomia sopra-aortica non complicata, anadamento rettilineo delle carotidi, placca fibrosa stabile], tutti possono essere impiegati tranquillamente; viceversa, nei casi complessi è meglio scegliere tra i vari presidi disponibili [Lo stent a cellule chiuse può essere scelto come prima opzione se so ha la necessità di una buona copertura della placca e prevenzione di un prolasso della stessa, su lesioni prone all’embolizzazione, placche soffici o lumghe ed inomogenee; Carotid Wallstent, Xact Abbott, Cristallo – se a prevalere è la problematica di un angolatura della biforcazione carotidea, per cui occorre rispettare il decorso dei vasi, allora la scelta cade su un presidio al nitinolo, Precise,Cordis – se a prevalere è la differenza di calibro tra carotide comune ed interna, la scelta si orienterà verso uno stent conico, Protegè eV3, Vivex Bard – se la stenosi è concentrica, molto calcifica, la scelta si orienta verso uno stent al nitinolo, a cellule chiuse, Xact, quello con maggiore forza radiale. – In presenza di più elementi da risolvere, lo stent ibrido offre più risposte, rispetto agli altri. – in caso di arco aortico difficile, la stabilità e il supporto sono fondamentali, ma anche la flessibilità dello stent può aiutare a portare a termine l’intervento; Wallstent, Cristallo, Vivex.].
La scelta dello stent deve tenere conto della lunghezza della stenosi [in genere centimetrica, anche se l’estensione della malattia può essere superiore], del diametro dell’arteria carotide interna e della comune [], del tipo di lesione da trattare [uno stent autoespandibile a cellule aperte garantisce una maggiore adattabilità ad una anatomia tortuosa, ma non ripara dalla protrusione della placca; se questa è a rischio, maggiore è la possibilità di una embolizzazione – lo stent a cellule chiuse garantisce una maggiore copertura della placca, ma ha una maggiore rigidità; questo viene utilizzato nelle placche a maggiore rischio embolico]. Una volta che lo stent è stato rilasciato, l’angiografia di controllo è finalizzata alla verifica del suo posizionamento, alla verifica della sua apertura. E’ accettata la persistenza di un restringimento della carotide, in quanto lo stent continuerà la sua dilatazione. E’ preferibile questo risultato ad eventuali complicazioni da sovradistensione [distacco di emboli, bradicardia].
Dopo l’impianto dello stent, per ottenere un risultato angiografico accettabile è necessaria una post-dilatazione; è questo un altro importante momento di rischio di embolizzazione [il diametro del palloncino è sottostimato, rispetto al calibro dello stent; il palloncino massimo da utilizzare è un 5mm, lungo 2 cm – non deve essere gonfiato a più di 10 atmosfere, previa somministrazione di atropina, per controbilanciare un eventuale riflesso ipotensivo e bradicardico – il gonfiaggio deve essere unico e breve, per evitare distacco di materiale]. Se una placca continua a protrudere tra le maglie dello stent, è meglio aggiungere un altro stent e non effettuare una PTA
L’angiografia di controllo finale serve a documentare il risultato dell’intervento [la prima arteriografia è focalizzata al solo tratto cervicale: la carotide interna è pervia, il flusso è regolare – in proiezione antero-posteriore e laterale, si effettua quella focalizzata allo studio dell’encefalo: si conferma che la circolazione cerebrale non ha subito insulti embolici – se non si vede flusso all’intero della carotide interna, occorre pensare ad una occlusione trombotica che va affrontata con l’aspirazione del materiale; un eventuale vasospasmo va trattato con nitroglicerina].
La rimozione del sistema di protezione cerebrale avviene secondo le istruzioni della casa costruttrice [deve avvenire sotto diretto controllo fluoroscopico – un’eventuale difficoltà può essere risolta ruotando la testa del paziente controlateralmente o ruotando il catetere guida]. L’introduttore lungo viene scambiato con uno corto, per facilitare la successiva chiusura dell’accesso, con un sistema di chiusura o con la compressione manuale.
Risultati clinici
L’endoarterectomia chirurgica è stata effettuata con successo, per molti anni; pertanto deve essere considerata il “gold standard”, o il punto di riferimento. Per dimostrare l’uguaglianza o la superiorità di una tecnica alternativa, bisogna criticamente valutare le complicazioni periprocedurali e l’efficacia clinica nel lungo periodo. IN questo caso l’obiettivo del trattamento è la sopravvivenza in assenza di stroke [sia minori, non disabilitanti o non permanenti, che i maggiori].
Per la CEA, sono stati definiti i criteri di sicurezza procedurali [incidenza di stroke nei pazienti sintomatici 6%, negli asintomatici 3& – Moore WS, Barnett HJM, Beebe HG, et al. Guidelines for carotid endoarterectomy: a multidisciplinary consensus statement from the ad hoc committee. Am H Assoc. Stroke 1995; 26: 188-201. – Nello studio NASCET, l’incidenza di stroke è stato del 6,7% nei pazienti sintomatici e 3% nei pazienti asintomatici]. Il confronto tra CEA e CAS (carotid artery stenting) non ha messo in evidenza sostanziali differenze: nel CAVATAS l’incidenza di stroke era superiore al 9% nei pazienti strattati con PTA, con lo stent impiegato solo nel 26% [Endovascular versus surgical treatment in patients with carotid stenosis in the carotid and vertebral and transluminal angioplasty study (CAVATAS): a randomized trial. Lancet 2001; 357: 1729-1791.]. Nello studio SAPPHIRE l’incidenza di stroke era del 4,5% e 6,6 nel gruppo trattato con CEA. Tali risultati sono superiori ai limiti fissati dalle linee guida, forse perché nei primi studi erano stati eliminati i pazienti più gravi, che invece qui sono stati trattati. [pazienti con oltre 80 anni, occlusione carotide controlaterale, recidiva dopo CEA, comorbilità cardiaca e polmonare. – Yadav J, et al. SAPPHIRE: stenting and angioplasty with protection in patients with high risk for endoarterectomy . Scientific comunications. 75th Scientific Session of Am H Ass. Chicago 2002.].
Uno dei vantaggi dell’approccio endovascolare è la totale assenza di lesioni sul nervo facciale e di problemi nella guarigione della ferita chirurgica, come nei pazienti trattati con radioterapia. L’incidenza delle complicanze negli accessi vascolari è diminuita con la miniaturizzazione dei presidi e con l’ingresso dei sistemi di chiusura.
Il confronto dell’efficacia clinica a lungo termine dello stent carotideo, rispetto al trattamento chirurgico, non è facile per la mancanza di dati comparabili; nello studio CAVATAS, l’incidenza dello stroke e morte, a 3 anni, era simile tra i due gruppi di pazientI; nello studio NASCET l’incidenza di stroke/morte era 15,8% a 2 anni; nel registro di Roubin era 11% nei pazienti sintomatici e 14% negli sintomatici. L’incidenza di restenosi dopo stent carotideo era inferiore al 10%.
Lo stenting carotideo sta emergendo come alternativa terapeutica, poco invasiva, per il trattamento delle stenosi carotidee; i risultati dei primi studi randomizzati hanno dimostrato sono sovrapponibili a quelli ottenuti con la chirurgia. Lo stent carotideo è da preferire nei pazienti con stenosi carotidea sintomatica, con oltre 80 anni, con comorbilità che li rendano a rischio chirurgico.
Effetti collaterali
PRECOCI
- Bradicardia: la stimolazione del bulbo carotideo può comportare un rallentamento del ritmo cardiaco; l’ipotensione può essere la conseguenza della bradicardia. Questo evento può essere affrontato solo farmacologicamente: 0,5-1mg di atropina in vena, almeno 1’ prima della dilatazione del catetere a palloncino.
- Crisi ipertensiva: di solito si risolve con una sedazione del paziente
- Spasmi dell’arteria carotide: può essere una complicanza dell’azione di sfregamento del filtro – possono essere sufficienti dei vaso dilatatori
- Trombosi acuta dello stent: secondaria ad una scarsa preparazione del paziente; aspirazione manuale e terapia anticoagulante.
- Embolizzazione periferica: oltre al controllo dei parametri vitali, va effettuata l’arteriografia di controllo. La sede più comune della lesione è a livello della porzione più distale dell’arteria carotide interna o della cerebrale media: una brusca interruzione di decorso di un vaso è facile da indentificare, più difficile per piccole e periferiche embolie. Va fatto un tentativo di ricanalizzare il vaso: il semplice passaggio di un filo guida 0,014” o una pTA può essere sufficiente a restaurare il flusso. I fattori di rischio che aumentano le possibilità di una embolizzazione periferica sono: una inadeguata preparazione del paziente con anti-aggreganti, una inadeguata anticoagulazione, un prolungato tentativo di conquistare la carotide comune, la presenza di placche ulcerate, una manipolazione aggressiva con il filo guida, un’eccessiva predilatazione o post-dilatazione, forzatura nell’oltrepassare una placca calcifica e serrata.
- Emorragia intracranica: preceduta da un mal di testa, l’emorragia può rivelarsi già in fase arteriografica o successivamente. Causata da un’eccessiva terapia anticoagulante, dalla presenza di un aneurisma cerebrale.
- Encefalopatia da contrasto: sindrome neurologica transitoria, secondaria ad un prolungamento temporale della procedura e dalla somministrazione di elevate dosi di mezzo di contrasto. Non si rilevano anomalie alla TC e all’arteriografia. Si risolve spontaneamente con l’idratazione e un’osservazione di 48-72 ore.
- Sindrome da iper-perfusione: mal di testa, nausea, vomito, deficit neurologici, emorragia intracranica si verificano in pazienti con una severa stenosi e scarso circolo collaterale che, improvvisamente, ricevono un nuovo e consistente afflusso di sangue. La sua insorgenza avviene nell’arco di poche ore. Terapia anticoagulante.
- Dissezione carotidea: la tortuosità dei vasi, lo scarso controllo della posizione del filtro, l’eccessiva manipolazione con filo guida e la post-dilatazione della parte distale dello stent sono alla base di tale alterazione. Occorre effettuare una PTA o prolungare lo stent.
- Perforazione della carotide: rarissima complicazione, secondaria ad una eccessiva post-dilatazione. Pretende lo stent ricoperto.
- Occlusione dell’arteria carotide esterna: rara, non produce sintomi, se esiste un buon circolo collaterale; la ricanalizzazione può essere tentata solo in presenza di sintomatologia. Anche in questo caso PTA.
- Ematoma dell’accesso vascolare: per l’eccessiva terapia anticoagulante somministrata e il calibro del materiale impiegato.
TARDIVE
- Restenosi dello stent
Dopo la procedura
Il monitoraggio del paziente continua anche nelle successive 12-24 ore. Il dosaggio dei medicamenti viene adattato agli esiti dei successivi controlli. Gli antiaggreganti vengono somministrati almeno per il primo mese, in forma di doppia antiaggregazione; per 6 mesi con un solo farmaco. I controlli eco-color-Doppler seguiranno con una cadenza semestrale.
Per approfondimenti invitiamo anche alla visione dell’articolo “Cosa serve per pianificare l’intervento di stent”.